
에이치엘비 “위암 글로벌 3상 추가 임상할 것”
“통계학적 유의미성 확보 못해…효능 충분히 입증할 것”
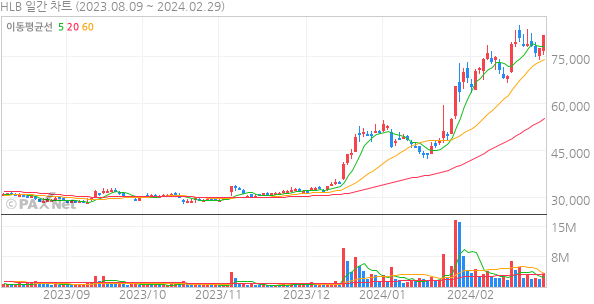
에이치엘비의 미국 자회사인 LSK바이오파마(이하 LSKB)는 항암제 ‘리보세라닙’의 위암 글로벌 3상 임상의 추가 임상을 실시하겠다고 28일 밝혔다.
지난 26일 발표한 리보세라닙의 글로벌 3상 주요 결과(탑라인)에 따르면 리보세라닙은 전체생존기간(OS)이 위약 대조군보다 높게 나왔으나 위약 대조군 대비 통계학적 유의미성을 확보하지 못했다. 이번 결과만으로는 미국 허가 신청이 쉽지 않을 것이라는 판단 하에 추가 임상시험을 진행하겠다는 것이다.
에이치엘비 관계자는 “1차 유효성 평가지표인 OS가 임상 목표치에 도달하지 못했지만, 2차 유효성 평가지표인 PFS가 통계학적으로 상당히 유의미한 결과가 도출됐다”며 “추가 임상을 통해 리보세라닙의 효능에 대해 충분히 입증하려는 것”이라고 설명했다.
또한 “현재 분석 중인 2차 유효성 평가지표 중 하나로 데이터가 확정된 PFS가 상당히 유의미한 수준으로 나온 만큼 진행성 또는 전이성 위암 환자를 대상으로 소규모 추가 임상을 실시할 계획”이라며, “추가 임상 환자규모는 데이터 최종 집계후 각국의 허가기관과 논의를 통해 정하겠다. 추가 임상 결과를 바탕으로 각 국가별 하위집단(Sub group) 분석을 통해 국가별 허가신청을 진행할 계획”이라고 밝혔다
에이치엘비는 무진행 생존기간(PFS)은 통계학적으로 대단히 유의미한 수준으로 나타났고 부작용도 경미한 수준으로 기존 연구사례와 다르지 않은 것으로 파악되고 있다고 설명했다. LSKB는 객관적 반응률(ORR), 질병조절율(DCR) 등 추가 데이터와 생존환자를 추가 분석해 전체 데이터를 9월말 유럽종양학회(ESMO)에서 공식 발표할 예정이다.
에이치엘비 관계자는 “디자인된 위암3차치료제로서의 임상 목표치 미도달에도 불구하고 PFS와 같은 주요 유효성 지표가 효능을 입증하고 있어서 현재 진행 중인 다양한 콤보 및 모노 임상에는 어떠한 영향도 없을 것”이라고 밝혔다.
한편, 지난 27일 임상결과에 대한 실망매물이 쏟아지며 에이치엘비와 계열사인 에이치엘비생명과학의 주가가 가격제한폭까지 하락했다.
지난 26일 발표한 리보세라닙의 글로벌 3상 주요 결과(탑라인)에 따르면 리보세라닙은 전체생존기간(OS)이 위약 대조군보다 높게 나왔으나 위약 대조군 대비 통계학적 유의미성을 확보하지 못했다. 이번 결과만으로는 미국 허가 신청이 쉽지 않을 것이라는 판단 하에 추가 임상시험을 진행하겠다는 것이다.
에이치엘비 관계자는 “1차 유효성 평가지표인 OS가 임상 목표치에 도달하지 못했지만, 2차 유효성 평가지표인 PFS가 통계학적으로 상당히 유의미한 결과가 도출됐다”며 “추가 임상을 통해 리보세라닙의 효능에 대해 충분히 입증하려는 것”이라고 설명했다.
또한 “현재 분석 중인 2차 유효성 평가지표 중 하나로 데이터가 확정된 PFS가 상당히 유의미한 수준으로 나온 만큼 진행성 또는 전이성 위암 환자를 대상으로 소규모 추가 임상을 실시할 계획”이라며, “추가 임상 환자규모는 데이터 최종 집계후 각국의 허가기관과 논의를 통해 정하겠다. 추가 임상 결과를 바탕으로 각 국가별 하위집단(Sub group) 분석을 통해 국가별 허가신청을 진행할 계획”이라고 밝혔다
에이치엘비는 무진행 생존기간(PFS)은 통계학적으로 대단히 유의미한 수준으로 나타났고 부작용도 경미한 수준으로 기존 연구사례와 다르지 않은 것으로 파악되고 있다고 설명했다. LSKB는 객관적 반응률(ORR), 질병조절율(DCR) 등 추가 데이터와 생존환자를 추가 분석해 전체 데이터를 9월말 유럽종양학회(ESMO)에서 공식 발표할 예정이다.
에이치엘비 관계자는 “디자인된 위암3차치료제로서의 임상 목표치 미도달에도 불구하고 PFS와 같은 주요 유효성 지표가 효능을 입증하고 있어서 현재 진행 중인 다양한 콤보 및 모노 임상에는 어떠한 영향도 없을 것”이라고 밝혔다.
한편, 지난 27일 임상결과에 대한 실망매물이 쏟아지며 에이치엘비와 계열사인 에이치엘비생명과학의 주가가 가격제한폭까지 하락했다.
ⓒ새로운 눈으로 시장을 바라봅니다. 딜사이트 무단전재 배포금지
관련기사
more

관련종목
# 추천 키워드
 Home
Home













